حیوانات آزمایشگاهی (6)
تزریق درون سیتوپلاسمی اسپرم چیست؟
شنبه, 14 اسفند 1400 19:59 نوشته شده توسط Site ManWhat is intracytoplasmic sperm injection (ICSI)?
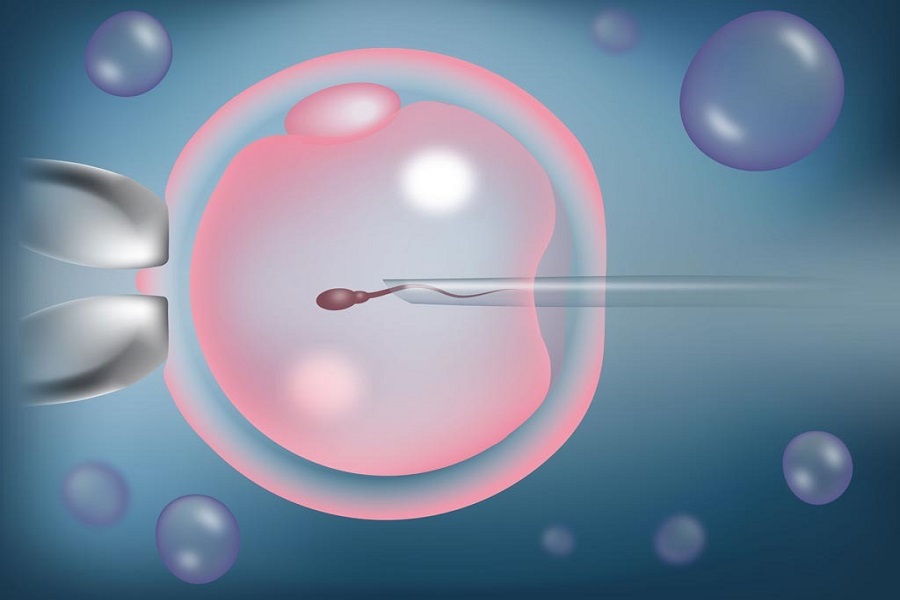
قبل از اینکه اسپرم یک مرد بتواند یک تخمک را بارور کند، سر اسپرم به خارج تخمک متصل شود.پس از اتصال اسپرم به تخمک، اسپرم از طریق لایه بیرونی به داخل تخمک(سیتوپلاسم) فشار می آورد، جایی که لقاح انجام می شود.
گاهی اوقات اسپرم به دلایل مختلف نمی تواند به لایه بیرونی نفوذ کند.لایه بیرونی تخمک ممکن است ضخیم باشدیا به سختی به آن نفوذ کند یا اسپرم قادر به شنا به سمت تخمک نباشد. در این موارد، روشی به نام تزریق اسپرم داخل سیتوپلاسمی (ICSI) همراه با لقاح آزمایشگاهی( IVF) برای کمک به بارور شدن تخمک انجام می شود. در طی ICSI ، یک اسپرم به طور مستقیم به سیتوپلاسم تخمک تزریق می شود.
ICSI چگونه کار می کند؟
دو روش برای بارور شدن تخمک توسط IVF وجود دارد: IVF و ICSI . در IVF ، 50000 یا بیشتر اسپرم متحرک در کنار تخمک در یک ظرف آزمایشگاهی قرار می گیرد. لقاح زمانی اتفاق می افتد که یکی از اسپرم ها وارد سیتوپلاسم تخمک شود. در فرایند ICSI ، یک سوزن کوچک به نام میکروپیپت برای تزریق یک اسپرم به مرکز تخمک استفاده می شود. با IVFیا ICSI، هنگامی که لقاح اتفاق می افتد، تخم بارور شده ( که اکنون جنین نامیده می شود) قبل از اینکه به رحم زن(رحم) منتقل شود، به مدت 1 تا 5 روز در آزمایشگاه رشد می کند.
چرا به ICSI نیاز داریم؟
ICSI برای غلبه بر مشکلات باروری کمک می کند، مانند:
مرد برای انجام لقاح مصنوعی ( تلقیح داخل رحمی [IUI]) ، یا IVF، اسپرم بسیار کمی تولید می کند.
اسپرم ممکن است در حالت عادی حرکت نکند.
ممکن است در اتصال به تخمک مشکل داشته باشد.
انسداد در دستگاه تناسلی مرد ممکن است از خروج اسپرم جلوگیری کند.
تخمک ها با IVF، بدون توجه به وضعیت اسپرم ، بارور نشده اند.
از تخمک های بالغ شده در شرایط آزمایشگاهی یا IVM استفاده شود.
از تخمک های فریز شده قبلی استفاده شود.
آیا ICSI کار خواهد کرد؟
ICSI 50% تا 80% تخمک ها را بارور می کند. اما مشکلات زیر ممکن است در طول یا بعد از فرایند ICSI رخ دهد:
ممکن است برخی یا همه تخمک ها آسیب دیده باشند.
ممکن است تخمک حتی پس از تزریق اسپرم به جنین تبدیل نشود.
رشد جنین ممکن است متوقف شود.
هنگامی که لقاح انجام می شود، شانس یک زوج برای به دنیا آوردن یک نوزاد مجرد، دوقلو یا سه قلو در صورت انجام با IVF یا بدون ICSI یکسان است.
آیا ICSI می تواند بر رشد کودک تاثیر بگذارد؟
اگر یک زن به طور طبیعی باردار شود، 1.5% تا3% احتمال دارد که نوزاد دارای یک نقص مادرزادی بزرگ داشته باشد. احتمال نقایص مادرزادی مرتبط با ICSI مشابه IVF است، اماکمی بیشتر از بارداری طبیعی است.
خطر کمی بالاتر نقایص مادرزادی ممکن است در واقع به دلیل ناباروری و نه درمان های مورد استفاده برای غلبه بر ناباروری باشد.
شرایط خاصی با استفاده از ICSI مرتبط است، مانند سندروم بکویث- ویدمن، سندرم آنجلمن، هیپوسپادیاس یا ناهنجاری های کروموزوم جنسی. در کمتر از 1% از کودکانی که با این تکنیک باردار شده اند رخ می دهد.
برخی از مشکلاتی که باعث ناباروری می شود ممکن است ژنتیکی باشد. به عنوان مثال ، کودکان پسری که با استفاده از ICSI باردار می شوند، ممکن است مشکلات ناباروری مشابه پدرشان داشته باشند.
مترجم: دکتر ندا ابراهیمیان
منبع: AMERICAN SOCIETY FOR REPRODUCTIVE MEDICINE, URL www.asrm.org
What is intracytoplasmic sperm injection (ICSI)?
روش های ترنس ژن سازی در حیوانات
شنبه, 14 اسفند 1400 17:30 نوشته شده توسط Site Manحیوان ترانس ژنتیک به حیوانی اطلاق می شود که در آن تغییر عمدی ژنوم بر خلاف جهش خود به خودی صورت گرفته است.DNA خارجی با استفاده از فناوری DNA نوترکیب به حیوان وارد می شود و سپس باید از طریق رده زایا منتقل شود هر سلول، از جمله سلول های زایا، حاوی همان مواد ژنتیکی اصلاح شده می باشد.
1-پیشینه تاریخی
قبل از توسعه ژنتیک مولکولی، تنها راه مطالعه تنظیم وعملکرد ژن های پستانداران، مشاهده ویژگی های ارثی یا جهش های خود به خودی بود. مدتها قبل از مندل هرگونه دانش ژنتیکی مولکولی، اصلاح انتخابی یک عمل رایج در میان کشاورزان برای افزایش صفات انتخابی ، به عنوان مثال، افزایش تولید شیر بود.
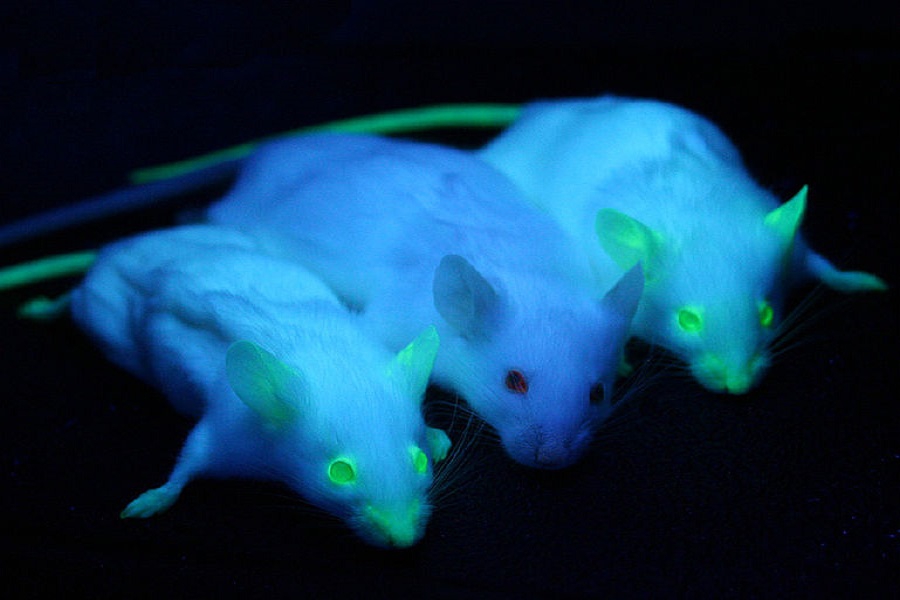
در طول دهه 1970، اولین موش کایمریک تولید شد(1974).سلولهای دو جنین مختلف از سویه های مختلف در مراحل اولیه رشد(هشت سلولی) با هم ترکیب شدند تا یک جنین منفرد را تشکیل دهند که در نهایت به یک موجود بالغ کایمریک تبدیل شده و ویژگی های هردو سویه را نشان می دهد.
مشارکت متقابل زیست شناسی تکوین و مهندسی ژنتیک امکان توسعه سریع تکنیک های ایجاد حیوانات ترانس ژنتیک را فراهم کرد. میکرو اینجکشن DNA ، اولین تکنیک موفقیت آمیز در پستانداران، ابتدا روی موش ها و سپس روی گونه های مختلف دیگر مانند موش ، خرگوش، گوسفند، خوک، پرندگان و ماهی ها اعمال شد.سپس دوتکنیک اصلی دیگر توسعه یافتند: روش های ترانس ژن با واسطه رتروویروس (1976) و انتقال ژن با واسطه سلول های بنیادی (ES) (1986) توسعه یافتند.
از سال 1981 زمانی که اصطلاح ترانس ژنتیک (1981)پا به عرصه علم گذاشت. توسعه سریعی در استفاده از حیوانات دستکاری شده ژنتیکی صورت گرفنه است زیرا محققان تعداد فزاینده ای از کاربردهای این فناوری را یافته اند.
2-روش های ایجاد حیوانات ترانس ژنیک
اندازه کوچک و هزینه کم اسکان در مقایسه با مهره داران بزرگتر، زمان تولید مثل کوتاه و ژنتیک کاملا مشخص آنها، موش ها به گونه اصلی مورد استفاده در زمینه ترانس ژن تبدیل شده است.
سه روش اصلی برای ایجاد حیوانات ترانس ژن عبارتند از: میکرو اینجکشن DNA ، انتقال ژن با واسطه سلولهای بنیادی جنینی و انتقال ژن با واسطه رتروویروس.
میکرو اینجکشن DNA :
این روش شامل میکرو اینجکشن مستقیم ژن انتخابی ( یک ژن یا ترکیبی از ژن ها) از یک عضو دیگر از همان گونه یا از یک گونه متفاوت به پیش هسته یک تخمک بارور شده است.این یکی از اولین روش هایی است که ثابت کرد در پستانداران موثر است. DNA معرفی شده ممکن است منجر به بیان بیش از حد یا کم بیان ژن های خاص یا بیان ژن های کاملا جدید برای گونه های حیوانی شود. با این حال ، قرار دادنDNA یک فرایند تصادفی است و احتمال زیادی وجود دارد که ژن معرفی شده خود را در محلی روی DNA میزبان قرار ندهد، که اجازه بیان آن را می دهد. تخمک لقاح یافته دستکاری شده به مجرای تخمک ماده گیرنده یا مادر فاستر منتقل می شود که با جفت گیری با یک نر وازکتومی شده به عنوان گیرنده عمل می کند.
مزیت: کاربرد به طور وسیع در انواع گسترده ای از گونه ها است.
انتقال ژن با واسطه سلولهای بنیادی جنینی:
این روش شامل وارد کردن توالی DNA مورد نظر با نوترکیبی هومولوگ در یک کشت آزمایشگاهی سلولهای بنیادی جنینی (ES) است. سلولهای بنیادی سلول های تمایز نیافته ای هستند که پتانسیل تمایز به هر نوع سلولی (سلولهای سوماتیک و زایا) را دارند و بنابراین یک موجود کامل را به وجود می آورند. سپس این سلولها در مرحله رشد بلاستوسیت به جنین وارد می شوند. نتیجه یک حیوان کایمریک است. انتقال ژن با واسطه سلول بنیادی جنینی) (ES روش انتخابی برای غیر فعال سازی ژن است که به اصطلاح روش Knock-out نامیده می شود.
این تکنیک برای مطالعه کنترل ژنتیکی فرایندهای تکوین از اهمیت ویژه ای برخوردار است.این تکنیک به ویژه در موش ها به خوبی کار می کند.
مزیت:امکان هدف گیری دقیق جهش های تعریف شده در ژن را از طریق نوترکیبی هومولوگ فراهم می کند.
انتقال ژن با واسطه رتروویروس ها:
برای افزایش احتمال بیان، انتقال ژن با واسطه یک حامل یا ناقل ، به طور کلی از یک ویروس یا یک پلاسمید به عنوان حامل استفاده می شود.
رتروویروسها معمولا به عنوان ناقلی برای انتقال مواد ژنتیکی به داخل سلول استفاده می شوند و از توانایی شان در آلوده کردن سلولهای میزبان با استفاده از این روش استفاده می کنند. فرزندان حاصل از این روش کایمریک هستند، یعنی همه سلولها حامل رتروویروس نیستند. انتقال ترانس ژنیک تنها در صورتی امکان پذیر است که رتروویروس در برخی از سلول های زایا ادغام شود.
برای هر یک از این تکنیک ها میزان موفقیت از نظر تولد زنده حیوانات حاوی ترانس ژن بسیار پایین است. به شرط اینکه دستکاری ژنتیکی منجر به سقط جنین نشود، نتیجه نسل اول (F1) از حیوانات است که باید برای بیان ترانس ژن آزمایش شوند.بسته به تکنیک مورد استفاده، نسل اول یا F1 ممکن است منجر به کایمر شود.هنگامی که ترانس ژن در سلولهای زاینده ادغام شد، به اصلاح کایمرهای خط زایا برای 10 تا 20 نسل هم خونی می شوندتازمانی که حیوانات ترانس ژنتیک هموزیگوت به دست آیند و ترانس ژن در هر سلول وجود داشته باشد. در این مرحله جنین های ترانس ژن را می توان منجمد کرد و برای لانه گزینی بعدی ذخیره کرد.
حیوانات ترانس ژنتیک در بیوتکنولوژی:
حیوانات ترانس ژن تنها یکی از پیشرفت ها در حوزه بیوتکنولوژی هستند. بیوتکتولوژی نحوه درک ما از فرایندهایی مانند مهندسی وساخت را تغییر داده است. این اصلاحات اکنون شامل استفاده از موجودات زنده یا اجزای آنها برای ساخت یا اصلاح محصولات ، تغییر خصوصیات گیاهان یا حیوانات، یا توسعه میکرو اورگانیسم ها برای مصارف خاص استفاده می شود. استفاده های جدید از تکنیک های DNA نوترکیب، تکنیک های همجوشی (fusion) سلولی، فناوری آنتی بادی تک کلونال و پلی کلونال وفرایندهای بیولوژیکی برای تولید تجاری ، تمایزات و روش های سنتی را تغییر داده است. دستکاری های ژنتیکی در سطح DNA دیدگاه های دیرینه درباره اینکه چه چیزی حیوان، گیاه و انسان در نظر گرفته می شود را تغییر داده است. به نوبه خود، این تغیییرات ارزابی روش های استفاده از حیوانات را دشوار تر کرده و تمایز بین تحقیقات خالص و کاربردی را پنهان کرده است.
در نظر گرفتن مقبولیت ایجاد گونه های حیوانی ترانس ژن خاص یا دستکاری ژنتیکی شامل تبادل DNA بین گونه ها و سلسله ها می تواند یک مسله ساده مراقبت از حیوانات یا یک تصمیم اجتماعی باشد.
ایجاد حیوانات ترانس ژن منجر به تغییر استفاده از گونه های درجه بالاتر به گونه های پایین تر می شود و همچنین استفاده تعداد حیوانات استفاده شده، تاثیر می گذارد.
نمونه ای از جایگزینی گونه های بالاتر با گونه های پایین تر ، امکان ایجاد مدل های بیماری در موش ها به جای استفاده از سگ ها یا نخستی های غیر انسانی است.
در دراز مدت ، کاهش تعداد حیوانات مورد استفاده، به عنوان مثال برای مطالعه بیماری های انسانی ، به دلیل ویژگی بیشتر مدل های ترانس ژن توسعه یافته امکان پذیرشده است. از سوی دیگر ، موفقیت روش منجر به استفاده از پتانسیل آن برای بررسی طیف وسیع تری از بیماری ها وشرایط شده است. استفاده واقعی از برخی از گونه ها ممکن است افزایش یابد، علاوه بر تعداد حیواناتی که به عنوان اهدا کننده درطی فرایندخاص قربانی می شوند. پتانسیل این فناوری همچنین امکان استفاده از گاو ، خوک، گوسفند و بز را به عنوان واحدهای فرآوری برای تولید پروتین یا اهدا کنندگان عضو فراهم کرده است.
فرایندهای تعاملی پیچیده پستانداران زنده در شرایط آزمایشگاهی قابل تکرار نیستند. با این حال ، حیوانات ترانس ژن ابزاری برای ارزیابی تغییرات ژنتیکی از نظر تغییرات آناتومیکی و فیزیولوژی در یک سیستم پیچیده فراهم می کنند. مدل های ترانس ژن در مقایسه با مدل های حیوانی سنتی دقیق تر هستند، به عنوان مثال ،موش های دارای تومور با افزایش حساسیت به رشد تومور ، نتایج مطالعات سرطان زایی را در بازه زمانی کوتاهتری بدست می آورد، بنابراین سیر توسعه تومور را در حیوانات مبتلا به آزمایش را کاهش می دهد. با این حال ، مدل ها معادل های دقیقی نیستند، بنابراین مانند هر سیستم دیگری باید در نتیجه گیری از داده ها دقت شود.
فهرستی از موارد حیوانات ترانس ژن برای بیوتکنولوژی:
-استفاده در تحقیقات پزشکی، حیوانات ترانس ژن برای شناسایی عملکرد فاکتورهای خاص در سیستم های همواستاتیک پیچیده از طریق بیان بیش از حد یا کم یک ژن ( با استفاده از ترانس ژن وارد شده) استفاده می شود.
-در سم شناسی : به عنوان حیوانات تست پاسخگو (تشخیص مواد سمی) می باشند.
-در ژنتیک تکوینی پستانداران کاربرد دارد.
-در بیولوژی مولکولی، آنالیز تنظیم بیان ژن از ارزیابی تغییر ژننیکی ویژه در همه سطح حیوان استفاده می شود.
-در صنعت داروسازی ، تولید هدفمند پروتین های دارویی، تولید دارو و آزمایش اثر بخشی محصول است.
-در بیوتکتولوژی : به عنوان تولید کننده پروتین های خاصی باشند.
-هورمون های دستکاری شده ژنتیکی برای تولید شیر، تولید گوشت.مهندسی ژنتیک دام و در آبزی پروری بر تغییرات فیزیولوژی و یا آناتومی حیوانات تاثیر می گذارد.روشهای کلونینگ تولید خطوط خونی خاص است.
-تکوین حیوانات بویژه تولید برای استفاده زنوگرافت تولید می شوند.
ملاحضات عمومی مهم شامل میزان تجربه بدست آمده در آزمایشگاه در رابطه با دامپروری ، استاندارد های صنعت برای تگهداری حیوانات ایجاد شده به طور خاص به عنوان ماشین های زنده برای تولید پروتین ها ، آنتی بادی ها و... است. چه واژه هایی برای توصیف و ارزیابی وضعیت حیواناتی که به عنوان واحدهای تولیدی استفاده می شوند مناسب است؟ شبیه سازی دالی تاکید بر پیشرفت های نوآورانه در علوم حیوانات بخشی از بیوتکنولوژی است. همچنین استفاده از زنوگرافت، حداقل در سطح بهداشت عمومی، رفاه حیوانات و انسان را غیر قابل تفکیک می کند.
مترجم: دکتر ندا ابراهیمیان
منبع:
AMERICAN SOCIETY FOR REPRODUCTIVE MEDICINE, URL www.asrm.org
Transgenic Animals
لقاح آزمایشگاهی چیست؟
شنبه, 14 اسفند 1400 08:37 نوشته شده توسط Site ManIn vitro fertilization
لقاح آزمایشگاهی (IVF) را می توان در حیوانات آزمایشگاهی مختلف با کشت همزمان تخمک و اسپرم به دست آورد. اول، تخمک گذاری در حیوانات ماده با تزریق هورمونی ایجاد می شود. سپس تخمک ها ی جمع آوری شده با کشت اسپرم در شرایط آزمایشگاهی در شرایط مناسب بارور می شوند. فرزندان حاصل از IVF معمولاً با انتقال جنین ها به دستگاه تناسلی (مجرای تخمدان یا رحم) ماده های باردار یا شبه باردار پس از کشت، جنین ها بدست می آیند تا آنها را به مراحل بعدی رشد تبدیل کنند.
IVF نه تنها برای به دست آوردن فرزندان حیوانات در خطر انقراض، حیوانات عقیم یا حیوانات با عملکرد تولید مثل پایین، بلکه برای مطالعه مکانیسم های لقاح یک روش کاملاً مفید است. انجماد جنین و اسپرم برای نگهداری از حیوانات مختلف، به عنوان مثال، حیوانات آزمایشگاهی نیز مهم هستند. در مورد حیوانات آزمایشگاهی، موش گونه ای است که IVF به ویژه زمانی مفید است که در یک زمان معین به تعداد زیادی جنین نیاز باشد.
همانطور که نرخ لقاح آزمایشگاهی 55 سویه موش را گزارش کردیم، هنوز برخی از سویه ها وجود دارند که نرخ لقاح پایین و / یا نرخ رشد پایین را در شرایط آزمایشگاهی نشان می دهند.
تولید فرزندان از جنین های بارور شده آزمایشگاهی در خرگوش (1959) و موش آزمایشگاهی (1974) گزارش شده است، هنوز هم بدست آوردن فرزندان مشتق شده از IVF با قابلیت تکرار بالا در حیوانات غیر از موش و خرگوش دشوار است. ما IVF موفقیت آمیز در ماستومی ها و ژربیل مغولی گزارش کردیم، اما هنوز فرزندانی از جنین های IVF بدست نیاورده ایم. تاکنون هیچ مقاله ای در مورد تولید موفق فرزندان حاصل از IVF در خوکچه هندی منتشر نشده است. باز تولید (تولید مجدد) نتایج حاصل از تولید موفق فرزندان در هامسترهای سوری که توسط آزمایشگاه های دیگر (1991) گزارش شده است، هنوز دشوار است.
بنابراین، ما باید به دنبال بهبودی برای IVF و تکنیک های مرتبط باشیم تا آنها را کارآمدتر و پایدارتر کنیم. در طول جستجو برای بهبود، ما بینش های گسترده تری را برای اسرار رشد حیوانات به دست خواهیم آورد.
مترجم: دکتر ندا ابراهیمیان
منبع: AMERICAN SOCIETY FOR REPRODUCTIVE MEDICINE, URL www.asrm.org
موش Nude و انواع آن در تحقیقات پیوند و سرطان
سه شنبه, 19 بهمن 1400 08:27 نوشته شده توسط Site Manموش آزمایشگاهی بدون شک یکی از پر استفاده ترین مدل ها در تحقیقات زیست پزشکی است. اندازه نسبتا کوچک آن ها، و مشابهت ژنتیکی و فیزیولوژیک به انسان ها، موش را به یک جاندار مدل بیماری های انسانی تبدیل کرده است. در دهه 1960 بود که برای اولین بار یک مقاله از موش های عریان (Nude mice)، که به عنوان موش های بدون تیموس (Athymic) نیز شناخته می شوند، نام برد. این یک سویه خاص موش است که فنوتیپی عمدتا بدون مو (Hairless) دارد. با گذشت 50 سال از زمان معرفی موش های Nude، این زمینه به علت پیشرفت تکنولوژی «هدف قرار دادن ژن ها (Gene targeting)» پیشرفت قابل ملاحظه ای داشته است. اما حتی با گذشت سال ها، موش های برهنه (Nude Mice) در زمینه های مختلف درمانی شامل سرطان و ایمونولوژی مورد استفاده قرار می گیرند.
بنابراین اگر شما همکاری دارید که از موش های Nude استفاده می کند، یا شما خودتان شروع به استفاده از این موش ها کرده اید، در اینجا برخی اطلاعات زمینه ای و تعدادی توصیه راجع به این مدل ها آورده ایم که دانستن آن ها می تواند مفید باشد.
موش های Nude چیستند؟
این موش ها ابزاری بی بدیل و بسیار ارزشمند در تحقیقات زیست پزشکی و کشف دارو هستند. به دلیل فنوتیپ نقص ایمنی که دارند ثابت شده که برای دریافت زنوگرافت (xenograft یا پیوند از گونه ای دیگر) و به ویژه تحقیقات سرطان بسیار مفید هستند. بنابراین، موش های برهنه یا Nude از یک تیموس سالم و بلوغ کارآمد سلول های T سیستم ایمنی (T cells) بی بهره اند ( این سلول ها عموما به صورت پراکنده و کم وجود دارند و بسیار ضعیف و شکننده هستند).
در مقایسه با موش های سویه طبیعی یا هتروزیگوت، موش های Nude به دلیل نداشتن تیموس، سلول های T بالغ تولید نمی کنند و تعداد لنفوسیت های در گردش آن ها کاهش یافته است. به علاوه، این فنوتیپ باعث شده که تولید آنتی بادی نیز در این موش ها وجود نداشته باشد. این ویژگی ها از این جهت بسیار مفید است که به طیفی از سلول ها یا بافت های خارجی اجاره می دهد تا به موش میزبان پیوند زده شوند.
با در نظر گرفتن همه جوانب ذکر شده، این ویژگی ها موش برهنه (Nude mice) را به یک مدل عالی برای پیوند لاین های سلولی زنوگرافت (به عنوان مثال پیوند سرطان های انسان به موش) تبدیل کرده است و این باعث شده تا بتوانیم مکانیسم های وخامت تومور را بهتر بشناسیم و تاثیر خالص دارو و یا درمان (از این جهت که دیگر سیستم ایمنی دخالتی در کاهش اندازه تومور ندارد) بر تومور را ارزیابی کنیم.
چه سویه هایی از موش Nude وجود دارد و تفاوت آن ها در چیست؟
در سال 1395 پژوهشگاه ابن سینا تعدادی موش Nude سویه BALB/C همخون از مبدا کشور آلمان به کشور وارد کرد و در حال حاضر این حیوانات در اتاق تمیز تخصصی کلاس A این پژوهشگاه نگهداری می شوند. تولید مثل این موش ها با دقت خاصی بر اساس جفت اندازی خواهر و برادر است تا ژنتیک خالص و همخون این حیوانات حفظ شود.
موش Nude BALB/C
این موش یک سویه همخون بوده که فاقد غده تیموس است و بنابراین توانایی تولید سلول های T را ندارد که در نتیجه دارای نقص سیستم ایمنی است. کنترل ژنتیکی این موش توسط موش هتروزیگوس از همین سویه انجام می شود.
مناسب برای تحقیقات ایمونولوژی سرطان و پیوند زنوگرافت
موش Athymic Nude
این موش برهنه دارای نقص ایمنی از موسسه ملی سلامت آمریکا سرچشمه گرفت و در ابتدا تصور می شد که یک موش BALB/c باشد. بعداً مشخص شد که همخون نبوده و به همین دلیل به عنوان غیر همخون نگهداری می شود و با هیچ استوک یا سویه ای مرتبط نیست. این حیوان فاقد تیموس است، قادر به تولید سلول های T نیست و در نتیجه دچار نقص ایمنی است.
مناسب برای تحقیقات ایمونولوژی سرطان و پیوند زنوگرافت
CD-1 Nude Mouse
از انتقال ژن برهنه از Crl:NU-Foxn1nu به یک موش CD-1 از طریق یک توالی آمیزش های پی در پی ضربدری و متقاطع از سال 1979 در آزمایشگاههای چارلز ریور ایجاد شد. حیوان فاقد تیموس است، قادر به تولید سلول های T نیست و در نتیجه دچار نقص ایمنی است.
مناسب برای تحقیقات ایمونولوژی سرطان و پیوند زنوگرافت
NIH-III Nude Mouse
به طور رایج با نام NIH-III شناخته می شود و در موسسه ملی سلامت ایالات متحده توسعه یافته است. علاوه بر ژن برهنه که منجر به عدم وجود تیموس و عملکرد سلول های T می شود، این موش دارای دو جهش دیگر در تنظیم عملکرد سیستم ایمنی است. اینها به عنوان نقص ایمنی مرتبط با کروموزوم X x (xid) و بژ (bg) تعیین می شوند. جهش xid بر بلوغ لنفوسیت های B مستقل از T تأثیر می گذارد. نشان داده شده است که هموزیگوت های bg دارای سلول های کشنده طبیعی (NK) معیوب هستند که در شرایط آزمایشگاهی برای سلول های تومور سیتوتوکسیک هستند. با این حال، میزان کمبود لنفوسیت B مستقل از T و سلول NK در NIH-III مشخص نشده است.
بدون مو هستند و پوست تیره رنگدانه دار نقطه ای دارند
مناسب برای تحقیقات ایمونولوژی سرطان و پیوند زنوگرافت
NU/NU Nude Mouse
این موش برهنه دارای نقص ایمنی، از موسسه ملی سلاما امریکا منشا گرفته و در ابتدا تصور می شد که یک موش BALB/c باشد. بعداً مشخص شد که این نژاد همخون نبوده و بنابراین به عنوان یک نژاد غیر همخون نگهداری می شود و با هیچ گونه استوک یا سویه ای مرتبط نیست. حیوان فاقد تیموس است، قادر به تولید سلولهای T نیست و بنابراین دچار نقص ایمنی است.
مناسب برای تحقیقات ایمونولوژی سرطان و پیوند زنوگرافت
پژوهشگاه ابن سینا با دارا بودن یک اتاق تمیز پرورش و یک اتاق تمیز پانسیون و کار بر روی موش های nude در حال تحقیق، بستر مناسبی را برای حضور پژوهشگران به وجود آورده است.
سفارش موش Nude از پژوهشگاه ابن سینا
021-22432020 (301) دکتر علیرضا حیدرنژاد
تست سمیّت جنینی بر روی جنین موش (Mouse Embryo assay یا MEA)
سه شنبه, 19 بهمن 1400 08:11 نوشته شده توسط Site Manاکثر وسایلی که در ART استفاده می شوند در طول مدت استفاده به طور مستقیم یا غیرمستقیم با گامتها (یعنی اسپرم و تخمک) و یا جنین تماس دارند. تست جنین موش (MEA) برای ارزیابی پتانسیل سمیّت جنینی وسایلی/موادی استفاده می شود که با گامت ها و جنین در ارتباط اند. در این تست که در 3 تکرار به انجام می رسد، وسیله/ماده مورد نظر در مجاورت جنین قرار داده شده و درصد جنین هایی که به مرحله بلاستوسیست می رسند مورد محاسبه و ارزیابی قرار می گیرد. استاندارد آزمایشگاه جنین شناسی میزان 80% بلاستوسیست از جمعیت ابتدایی می باشد.
این تست برای ارزیابی وسایل و یا موادی که در مرحله ابتدایی تولید قرار دارند بسیار در امر تحقیق و توسعه محصول ابتدایی کاربرد دارد. همچنین طبق پروتکل های سازمان غذا و دارو امریکا و اداره کل تجهیزات پزشکی ایران، هر وسیله/ماده تولید شده برای استفاده در IVF باید برای هر LOT از تولید محصول، گواهی عدم سمیّت جنین ارائه کند.
از آنجاییکه جنین های موش هیبرید نسل اول بسیار نسبت به مواد سمیت زا برای جنین حساس می باشند، لذا این تست حتما باید بر روی جنین های مذکور صورت پذیرد.
آزمایشگاه پیشرفته جنین شناسی حیوانات آزمایشگاهی پژوهشگاه ابن سینا در محل دانشگاه شهید بهشتی با هدف کمک به امر تولید و همچنین ارزیابی تمامی موارد تولید شده برای استفاده در IVF بالینی انسان مورد بهره برداری قرار گرفته است و در این راستا آماده هرگونه همکاری همکاری با تمامی شرکت های دانش بنیان است که در زمینه تولید محیط های کشت، ساخت وسایل فریز گامت و جنین، تولید پتری دیش های کشت جنین و سایر وسایل/موارد مورد استفاده در زمینه IVF فعالیت می کنند.
برای سفارش تست سمیت جنین موش (Mouse embryo assay) لطفا با این شماره ها در تماس باشید:
021-22432020 (داخلی 301)
09161911265 دکتر علیرضا حیدرنژاد
آغاز به کار آزمایشگاه کنترل کیفی محصولات حوزه جنین شناسی و ناباروری
سه شنبه, 19 بهمن 1400 07:41 نوشته شده توسط Site Manپژوهشگاه ابن سینا در راستای کمک به پیشبرد امر تولید و همچنین آزمون مواد و وسایل تولید شده مرتبط با IVF پیش از استفاده در کلینیک های درمان ناباروری، اقدام به تاسیس یک آزمایشگاه مجهز و پیشرفته در خصوص جنین شناسی حیوانات آزمایشگاهی کرده است. این آزمایشگاه با دارا بودن تمامی امکانات لازم، آماده ارائه خدمت به شرکت های دانش بنیان در جهت انجام فرآیندهای تحقیق و توسعه بوده و نیاز شرکت های مذکور به داشتن یک آزمایشگاه جنین شناسی پر هزینه را برطرف خواهد نمود و از این رو به افزایش سرعت تولید و ارائه محصول بی نقص نهایی به بازار کمک شایان توجهی خواهد نمود. از این رو آزمایشگاه جنین شناسی حیوانات آزمایشگاهی پژوهشگاه ابن سینا کار خود را با ارائه آزمون سمیّت جنین موش (Mouse embryo assay یا MEA) آغاز نموده است.
همچنین این آزمایشگاه آماده ارائه خدمت به اعضای هیئت علمی و دانشجویان ایشان در راستای پیش برد پایان نامه ها و طرح های تحقیقاتی در زمینه جنین شناسی حیوانات آزمایشگاهی است.
از دیگر اقدامات آتی این مجموعه می توان به آموزش دانشجویان داخلی (بیولوژی تولید مثل) و بین الملل در زمینه تکنیک های مورد استفاده در حیطه جنین شناسی شامل تزریق درون سیتوپلاسمی اسپرم، بیوپسی از جنین، کشت و ارزیابی جنین، لقاح آزمایشگاهی، اعمال جراحی روتین بر حیوانات آزمایشگاهی و ... اشاره کرد.
ارتباط با مدیریت آزمایشگاه های حیوانات پژوهشگاه ابن سینا
021-22432020 داخلی 301
09161911265 دکتر علیرضا حیدرنژاد